Продолжение.
Паразиты. Энтеробиоз, трихоцефалез, капилляриоз.
Паразиты. Стронгилоидоз, гнатостомоз, аскаридоз.
Паразиты. Нематоды.
Helicobacter Pylori, часть 2
Helicobacter Pylori, часть 1
Рак и СПИД
Профилактика и подготовка к терапии
Заболевания вызванные паразитами
Симптомы наличия паразитов в организме
Паразиты – кто они?
Начало.
Токсокароз
Токсокароз является заболеванием, о котором, несмотря на широкое распространение и важную роль в патологии, особенно у детей, практические врачи знают весьма немного. Симптоматика его очень разнообразна, поэтому с ним могут встретиться врачи самых разных специальностей: педиатры, терапевты, окулисты, гематологи, гастроэнтерологи, невропатологи и другие.
Еще в 1911 г. F. Fulleborn высказал предположение о возможности паразитирования у человека несвойственных ему видов аскаридат с развитием аллергических реакций. В 1952 г. P. Beaver назвал феномен миграции личинок гельминтов животных у человека «larva migrans» (мигрирующие личинки) и утвердил этот термин как диагностическую единицу. «Larva migrans» – это большая группа зоонозных болезней, характеризующаяся следующими особенностями:
человек для их возбудителя – несвойственный хозяин;
возбудители в организме человека не достигают половозрелого состояния;
симтомокомплекс обусловлен миграцией личинок или взрослых гельминтов в коже или внутренних органах человека.
В зависимости от преобладающих симптомов выделяют кожную, висцеральную и глазную формы larva migrans. Позднее, в 1969 г., P. Beaver предложил в тех случаях, когда известен возбудитель, обозначать заболевание не расплывчатым термином «мигрирующая личинка», а конкретным названием, происходящим от названия возбудителя (дирофиляриоз, гнатостомоз, ангиостронгилез, капиляриоз, спарганоз и др.). Инвазию, вызываемую аскаридатами собак (Toxocara canis), он назвал токсокарозом.
Морфология и жизненный цикл возбудителя
Возбудитель токсокароза – нематода семейства Anisakidae (Skrjabin et Korokhin, 1945) рода Toxocara (Stiles, 1905). Известны три вида токсокар: Tocsocara canis (Werner, 1782) – гельминт, поражающий главным образом представителей семейства псовых, Toxocara mystax (Zeder, 1800) — гельминт семейства кошачих, который иногда в англоязычных странах называют Tocsocara cati и Toxocara vitulorum (гельминт, поражающий коров) роль которого пока не изучена
Роль Т. canis в патологии человека доказана, а роль Т. mystax еще обсуждается, поэтому в настоящее время термин «токсокароз» подразумевает только заболевание человека, вызываемое Toxocara canis.
Toxocara canis – нематода, самка которой имеет длину 6-8 см, самец – 4-10 см. Одним из важных дифференциальных морфологических признаков токсокар являются вздутия кутикулы на головном конце, образующие боковые крылья размером 2.3 на 0.3 мм.
Яйца токсокар почти круглой формы. Они крупнее оплодотворенных яиц аскарид – соответственно 65-75 и 50-70 мкм. Наружная оболочка яиц толстая, плотная, мелкобугристая, напоминающая поверхность наперстка, цвет ее – от светло-коричневого до темно-коричневого. Внутри незрелого яйца расположен шаровидный темный бластомер, заполняющий почти все яйцо. В зрелом яйце содержится живая личинка.
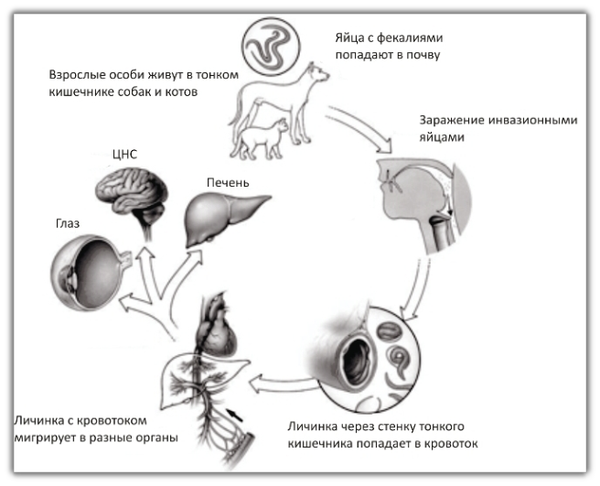
Т. canis обычно паразитирует у собак, волков, лисиц, песцов и других представителей семейства псовых. Взрослые паразиты локализуются в тонком кишечнике и желудке облигатных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4 мес., максимальная 6 мес. Самка Т. canis откладывает более 200 тыс. яиц в сутки. Поскольку зараженное животное носит в себе целую колонию токсокар, оно загрязняет окружающую среду миллионами яиц в сутки.
Яйца выделяются незрелыми (на стадии развития одного бластомера). Срок созревания яиц зависит от температуры окружающей среды и влажности. Зрелое яйцо содержит личинку, совершившую две линьки. В почве яйца длительное время сохраняют жизнеспособность. Широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
Для человека токсокароз – зоонозная инвазия. Она характеризуется тяжелым, длительным и рецидивирующим течением, полиморфизмом клинических проявлений, обусловленных миграцией личинок токсокар по различным органам и тканям. Заражение человека происходит при проглатывании зрелых яиц токсокар. В проксимальном отделе тонкого кишечника из яиц выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца. Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают пункта, где диаметр сосуда их не пропускает (диаметр личинки 0,02 мм), и здесь они покидают кровяное русло. Личинки токсокар оседают в печени, легких, сердце, почках, поджелудочной железе, головном мозге, глазах и других органах и тканях. Здесь они сохраняют жизнеспособность в течение длительного времени (месяцы, годы). Личинки, осевшие в тканях, пребывают в «дремлющем» состоянии, а затем под влиянием каких-то факторов активизируются и продолжают миграцию. С течением времени часть личинок инкапсулируется и постепенно разрушается внутри капсулы.
Патогенез и патология
Мигрируя в организме человека, личинки травмируют ткани, оставляя геморрагии, некрозы, воспалительные изменения. В секретах и экскретах личинок содержатся вещества, обладающие антигенной активностью (экзоантигены). Соматические антигены (эндоантигены) попадают в организм человека после разрушения личинки. Антигенное воздействие вызывает развитие аллергических реакций немедленного и замедленного типа. Судя по клинико-лабораторным показателям, поступление антигенов в организм человека происходит неравномерно и усиливается при возобновлении миграции после выхода из «дремлющего» состояния либо после гибели паразита.
В развитии аллергической реакции немедленного типа первый момент встречи организма человека с личинкой не вызывает видимых проявлений, основные клинические симптомы связаны со второй фазой, так называемой «реакцией поздней фазы» в виде отека, эритемы кожи и увеличения резистентности дыхательных путей к вдыхаемому воздуху. В «реакции поздней фазы» принимают участие тучные клетки, базофилы, а также нейтрофилы. В это время повышается уровень гистамина и хемотаксического фактора нейтрофилов и других клеток.
Основную роль в механизме противопаразитарного иммунитета играют эозинофилы. Эти клетки осуществляют защиту организма человека в содружестве с иммуноглобулином Е, уровень которого неизменно повышается при токсокарозе, а также с тканевыми базофилами, макрофагами. Как известно, пролиферация эозинофилов регулируется Т-лимфоцитами.
Механизм привлечения эозинофилов очень сложен и многократно дублируется. В нем принимают участие лимфокины, выделяемые сенсибилизированными лимфоцитами, низкомолекулярный хемотаксический фактор, продуцируемый нейтрофилами при взаимодействии их с иммунными комплексами, лейкотриены, продуцируемые лимфоцитами, нейтрофилами, тканевыми базофилами.
Тканевые базофилы у человека находятся в слизистых оболочках, коже, легких. На пути миграции личинки токсокар постоянно соприкасаются с этими и другими клетками.
Количество тканевых базофилов зависит от степени сенсибилизации организма антигенами. Тканевые базофилы выделяют активные амины (гепарин, гистамин), которые препятствуют свертыванию крови, расширяют сосуды, способствуют миграции клеток в очаг повреждения. В сочетании с лейкотриенами и другими медиаторами они вызывают основные клинические симптомы аллергии: гиперемию, зуд кожи, крапивницу, бронхоспазм, что и характерно для токсокароза.
Процесс освобождения активных аминов происходит при соединении IgE-антител с антигенными детерминантами клеток, активации комплемента, агрегации тромбоцитов или активации кининовой системы, что, по-видимому, приводит к тромбоцитопении при токсокарозе. Полинуклеары на фоне этого процесса повреждают мелкие кровеносные сосуды. При этом выделяются эндогенные пирогены, которые часто вызывают повышение температуры тела. Иммунные комплексы привлекают в очаг поражения эозинофилы, в результате чего образуются эозинофильные инфильтраты. Эозинофилы частично разрушают иммунные комплексы, смягчая этим тяжесть патологических реакций в тканях.
Реакция иммунных комплексов, наряду с выше указанными факторами, ответственна за формирование лихорадочной реакции, крапивницы, генерализованной лимфаденопатии.
Сенсибилизированные Т-лимфоциты, скопившиеся вокруг личинки, выделяют лимфотокины, привлекают и активируют макрофаги и другие клетки, которые включаются в процесс формирования гранулем.
Гранулемы при токсокарозе могут образовываться в любом органе и ткани за счет механизмов реакции замедленного типа. В центре гранулемы имеется зона некроза, по периферии — большое количество эозинофилов, а также гистоциты, нейтрофилы, лимфоидные, эпителиоидные клетки и макрофаги. Многочисленные гранулемы при токсокарозе находятся в печени, легких, а также в поджелудочной железе, миокарде, мезентериальных лимфатических узлах, головном мозге.
Таким образом, гистоморфологически токсокароз представляет собой диссеминированный эозинофильный гранулематоз как проявление аллергической реакции замедленного типа.
Заражение паратенических хозяев зрелыми яйцами токсокар приводит в течение нескольких дней к поражению печени с выраженной эозинофильной инфильтрацией интерстициальной ткани. В печени при этом образуется много гранулем с личинками и без них. Позднее по периферии клеточного слоя гранулемы с личинкой образуется фиброзная капсула. Так же быстро формируются гранулемы в легких, что приводит к гиперемии и отеку легочной ткани, активной лимфоидной реакции, а затем к возникновению пневмонии и альвеолита. В течение первых дней после заражения личинки попадают в головной мозг, почки, мышцы и другие органы и ткани.
В селезенке развиваются пролиферативные изменения в фолликулах. В корковом слое почек образуются лейкоцитарные скопления с наличием множества эозинофилов, паразитарные гранулемы. В миокарде возникают клеточные инфильтраты и экстравазаты. По истечении первой недели после заражения число личинок в этих органах значительно снижается. Личинки сохраняют жизнеспособность многие месяцы и годы, а их распределение в органах и тканях продолжает меняться. Число личинок в печени значительно больше при суперинфекциях и реинфекциях, чем при заражении низкими дозами или при обычном первичном заражении. Все вышеперечисленное в какой-то степени происходит в организме человека, который также является паратеническим хозяином токсокар.
Личинка в организме человека может выживать до 10 лет. Эта, как бы противоречащая выраженному иммунному ответу хозяина жизнеспособность личинки связана с выделением ею маскирующей субстанции, способной защитить личинку от агрессии эозинофилов и антител хозяина при помощи сложной реакции, в результате которой предотвращается их контакт с эпикутикулой личинки.
Формирование иммунного ответа – основной защитной реакцией организма – является главным механизмом патогенеза гельминтов вообще, и токсокароза в частности. Иммунологические реакции, переходя границы адекватного иммунного ответа, становятся иммунопатологическими и являются причиной формирования патологического процесса.
Следовательно, все патологические проявления при токсокарозе связаны в основном с аллергическими реакциями немедленного и замедленного типа. Однако, остается еще много неразрешенных вопросов в патогенезе токсокароза, например, механизм возникновения токсокароза глаз. Одна из гипотез высказана L.T. Glickman и P.W. Schantz, которые считают, что при низкой интенсивности инвазии личинками токсокар, суммарное антигенное воздействие на организм недостаточно, чтобы вызвать развитие аллергических реакций, гранулематозные процессы, эозинофилию, поэтому личинки свободно мигрируют по органам и тканям и попадают в органы зрения. При интенсивном заражении личинки попадают в «ловушку» иммунной и воспалительной реакций. Но на этом фоне иммунной защиты могут развиваться не только висцеральная форма, но и сочетанная патология в виде висцерального и глазного токсокароза одновременно.
Клиника
Спектр клинических проявлений зависит от интенсивности заражающей дозы, частоты реинфекций, распространения личинок в тех или иных органах и тканях, а также степени иммунного ответа хозяина. Токсокароз характеризуется длительным рецидивирующим течением (от нескольких месяцев до нескольких лет), что связано с периодическим возобновлением миграции личинок токсокар. Редкие летальные случаи при токсокарозе связаны с миграцией личинок в миокард и важные в функциональном отношении участки центральной нервной системы.
Соотношение частоты различных клинических форм токсокароза изучено пока недостаточно, однако по данным Центра по борьбе с болезнями в США на висцеральный токсокароз приходится 20%, глазной – 67%, бессимптомный – 13% от общего числа зарегистрированных в 1981 г. случаев. В Словакии (1993) на висцеральный токсокароз приходится 36%, глазной – 26% случаев.
В последние годы было установлено (Лысенко А.Я., Фельдман Э.В., Рыбак Е.А.), что токсокароз у детей приводит к снижению эффективности вакцинации и ревакцинации против кори, дифтерии и столбняка. У незараженных детей средние показатели титров антител часто превышают защитный уровень еще до ревакцинации, тогда как у зараженных личинками токсокар этот уровень и после ревакцинации остается ниже защитного. По сравнению с другими гельминтозами (энтеробиоз, аскаридоз) T. canis обладает наиболее активным поливалентным иммуноподавляющим действием.
Висцеральный токсокароз
Висцеральным токсокарозом болеют как дети, так и взрослые, хотя у детей это заболевание встречается чаще. Развитие висцерального токсокароза происходит вследствие заражения большим числом личинок и ассоциируется, например, у детей, с привычкой брать землю в рот. Основными симптомами токсокароза являются рецидивирующая лихорадка, легочный синдром, увеличение размеров печени, лимфаденопатия, эозинофилия, гипергаммаглобулинемия.
По нашим данным, у больных токсокарозом детей температура повышается обычно в полдень или вечером, сопровождаясь небольшим ознобом. Температурная реакция, как правило, наблюдается в период легочных проявлений (62% случаев). Синдром поражения легких встречается у 65% больных висцеральным токсокарозом и варьирует в широких пределах: от катаральных явлений до тяжелых астмоидных состояний. У больных наблюдаются рецидивирующие катары, бронхиты, бронхопневмонии. Беспокоит сухой кашель, частые приступы ночного кашля, в некоторых случаях – тяжелая одышка с астматическим дыханием и цианозом. При аускультации выслушиваются сухие, нередко влажные хрипы. При токсокарозе известны случаи развития тяжелых пневмоний, которые протекали с осложнениями и заканчивались летальными исходами. У нескольких больных, находящихся под нашим наблюдением и длительно страдавших бронхиальной астмой, удалось установить токсокарозную этиологию болезни, выявив высокий уровень специфических антител. Повторные курсы специфической терапии привели к купированию специфических проявлений болезни и постепенному полному выздоровлению. Подобное исследование, проведенное в Нидерландах, показало, что среди детей больных бронхиальной астмой или рецидивирующим бронхитом токсокароз выявляется с частотой 19.2% (в контрольной группе – 9.9%).
При рентгенологическом исследовании по нашим данным у 33.2% больных выявляются множественные или единичные эозинофильные инфильтраты, усиление легочного рисунка, картина бронхолёгочной инфильтрации.
Наряду с синдромом поражения легких очень часто (до 80 % по нашим наблюдениям) отмечается увеличение размеров печени. Печень при пальпации уплотнена, гладкая, часто напряженная. Примерно у 20 % больных увеличена селезенка, у 67 % – лимфатические узлы, вплоть до системной лимфаденопатии, особенно часто у детей. Лимфоузлы небольшого размера, безболезненные, не спаяны с окружающими тканями.
Кроме перечисленных проявлений у 46% наблюдаемых нами больных отмечался абдоминальный синдром (боли в животе, вздутие живота, тошнота, иногда рвота, диарея).
У 32 больных заболевание сопровождается разнообразного типа рецидивирующими высыпаниями на коже (эритематозные, уртикарные). Пальпаторно в местах высыпаний обнаруживаются небольшие уплотнения. Обследование на токсокароз детей с диагнозом «экзема», проведенное во время уже упомянутого исследования в Нидерландах, показало, что среди них 13.2 % имеют высокие титры специфических антител к токсокарам.
В отдельных случаях токсокароз протекает с развитием миокардита, по-видимому, аллергической природы. Описаны также эозинофильные панкреатиты, различные поражения почек, эозинофильные гранулемы в слизистой прямой кишки.
В последнее время некоторые исследователи наряду с висцеральным и глазным выделяют неврологическую форму токсокароза. При миграции личинок токсокар в головной мозг выявляются признаки поражения центральной нервной системы в виде конвульсий типа «petit mal», эпилептиформных припадков, парезов и параличей. Следует отметить, что частота высоких титров противотоксокарных антител у пациентов с эпилептическими припадками выше, чем в контрольной группе здоровых лиц, однако она одинакова у тех, у кого причина эпилептических припадков известна и неизвестна. Скорее всего, эпилепсия является не следствием, а лишь предрасполагающим к заражению токсокарозом фактором. Заражение токсокарозом вызывает также различные неврологические нарушения, проявляющиеся в изменении поведения: гиперактивность и аффекты в широком спектре поведенческих реакций – обучение, исследование внешней среды, решение комплекса проблем по выходу из сложной ситуации. Увязка таких явлений непосредственно с токсокарозом весьма проблематична, однако в одном из исследований показана связь затруднений при чтении, невозможности сосредоточиться и низкого уровня интеллекта с заболеванием дошкольников токсокарозом (1984 г.). Проведенное в Нью-Йорке обследование детей 1-15 лет показало, что инвазированные токсокарами дети имели существенные отклонения от здоровых детей во многих нейропсихологических тестах, моторной и познавательной функции.
Глазной токсокароз
Развитие глазного токсокароза связывают с заражением человека минимальным количеством личинок. Пациенты с глазным токсокарозом обычно старше, чем с висцеральным, иммунный ответ на заражение не так ярок, титры специфических противотоксокарных антител у них, как правило невысокие.
Первые случаи глазного токсокароза были выявлены в начале 50-х гг. нашего столетия, когда H. Wilder, проведя гистологическое исследование 46 глаз, энуклеированных у детей в связи с ретинобластомой (24 случая), болезнью Коатса, эндофтальмитом, в 24 случаях обнаружил личинки нематод или гиалиновые капсулы. Характерным изменением был эозинофильный абсцесс с некротическим центром. В 20 из этих 24 случаев заболевание клинически расценивалось как ретинобластома. В последующем токсокароз глаза начали диагностировать в разных странах с достаточным постоянством. Клинически у детей заболевание проявляется в виде косоглазия, снижения зрения, лейкокории. Личинки могут быть обнаружены при офтальмологическом исследовании, например, в области зрительного нерва или макулярной области.
Все случаи токсокароза глаза подразделяются на 2 основные группы: солитарные гранулемы и хронические эндофтальмиты с экссудацией. Практически всегда токсокарозом поражается только один глаз. При глазном токсокарозе обнаруживают, как правило, не более одной личинки.
Своеобразную форму поражения глаз при токсокарозе описали Hogan и соавторы в 1965 г. Личинка была обнаружена на периферии сетчатка у ребенка с хроническим парс-планитом. В стекловидном теле находился экссудат в виде «снежных шаров».
По данным некоторых авторов (Perkins, 1966) 10 % случаев хронического увеита связано с токсокарозом глаза.
В некоторых случаях (например, при интраретинальной миграции личинки) во время офтальмоскопии можно заметить движение личинки, а у пациента в поле зрения возникает мигрирующая скотома.
Поражение зрительного нерва личинкой токсокары может привести к односторонней слепоте. При этом диск и окружающая сетчатка инфильтруются лимфоцитами и эозинофилами, плазматическими клетками. Суммируя имеющиеся данные о поражении глаз при токсокарозе офтальмолог В.М. Чередниченко (1985 г.) выделяет следующие их формы:
гранулемы в заднем отделе глаза,
периферические гранулемы,
увеит,
парс-планит,
хронический эндофтальмит,
абсцесс в стекловидном теле,
неврит зрительного нерва,
кератит,
мигрирующие личинки в стекловидном теле.
В большинстве публикаций глазной токсокароз описан у детей.
Надежных методов диагностики глазного токсокароза не существует. Во многих случаях диагноз выясняется только при гистологическом исследовании. Brown (1970) сообщил, что из 245 энуклеированных им глаз в связи с диагнозом ретинобластомы, в 88 (35.9 %) обнаружена личинка токсокары. Дополнительными методами диагностики глазного токсокароза являются иммунологические реакции (которые не всегда в случаях глазного токсокароза бывают информативными), ультразвуковое и рентгенографическое исследование. В 1977 г. предложено в сомнительных случаях ретинобластомы проводить серологическое исследование на токсокароз пунктата передней камеры, а в 1979 г. — биоптата стекловидного тела.
Распространённость Токсокароза. Нами проведены расчеты оценочного числа лиц, больных висцеральным токсокарозом в РФ. Ожидаемое число больных среди детей в возрасте до 14 лет составляет 184 тыс. человек, в возрастной группе старше 14 лет – 366 тыс. Всего расчетное число больных токсокарозом может быть близким к цифре 550 тыс. человек, что составляет 380 на 100 тыс. населения. Для сравнения напомним, что аналогичный показатель при аскаридозе в 1993 г. составил 71.8.
Совершенно очевидно, что глазной токсокароз еще более недовыявляется, чем висцеральный. Это следует из сравнения с данными в США, где среди 700-1000 ежегодно регистрируемых Центром по борьбе с болезнями случаев токсокароза (по мнению специалистов Центра, эти сведения далеко не полные) на глазной токсокароз приходится 500-600 случаев, т.е. 67 %.
Лабораторные показатели. Одним из ведущих и наиболее постоянных проявлений висцеральной формы токсокароза является стойкая длительная эозинофилия вплоть до развития эозинофильно-лейкемоидных реакций крови. Обычно относительный уровень эозинофилов превышает 30%, а в отдельных случаях может достигать 90%. Высокий уровень эозинофилии отмечается также в некоторых случаях глазного токсокароза (до 44 %), но в целом она менее выражена и не столь постоянна. Общее количество лейкоцитов также повышается до 15-20х109/л, а в некоторых случаях – до 80х109/л. Эозинофилия может сохраняться в течение нескольких месяцев и даже лет.
По нашим данным, у больных висцеральной формой токсокароза (детей и взрослых) заболевание протекало с высокой эозинофилией периферической крови и у многих с повышением содержания лейкоцитов. По тяжести течения болезни можно выделить субклиническое, легкое и среднетяжелое, причем заболевание обычно протекает тяжелее у детей по сравнению со взрослыми. Средние показатели содержания лейкоцитов и эозинофилов у детей и взрослых различаются, имеется также тенденция к их увеличению по мере утяжеления течения болезни. Если содержание эозинофилов при субклиническом течении токсокароза у детей колебалось от 8 до 37%, при легком – от 12 до 74%, при среднетяжелом – от 20 до 80%, при тяжелом – от 60 до 79%, то у взрослых в этих же группах выявлены еще более высокие показатели. Так, при субклиническом течении токсокароза эозинофилия у взрослых составляла от 8 до 80%, при легком течении – от 13 до 84%, а при среднетяжелом – от 39 до 85%. Многие исследователи отмечают, что при прочих равных условиях у детей с токсокарозом уровень эозинофилии бывает выше, чем у взрослых.
В пунктате костного мозга выявляется эозинофильная гиперплазия, СОЭ обычно повышена, иногда значительно. При длительном течении болезни постепенно усиливается анемизация больных, уменьшается число эритроцитов, снижается уровень гемоглобина. Уровень общего белка сыворотки крови возрастает за счет глобулинов. В раннем периоде болезни преобладают иммуноглобулины класса М, позднее выявляются иммуноглобулины класса G. Особенно резко нарастает уровень иммуноглобулинов класса Е, который превышает норму у отдельных больных в 25-30 раз. При токсокарозе глаза эти явления выражены не столь ярко и могут отсутствовать.
Диагностика. Прижизненный паразитологический диагноз токсокароза практически невозможен, поскольку обнаружить мигрирующие личинки трудно, а идентифицировать их по гистологическим срезам весьма непросто. Тем не менее, окончательный паразитологический диагноз токсокароза ставят без сомнений только при обнаружении личинок в биоптатах тканей. Ограниченная возможность паразитологической диагностики приводит к тому, что ведущими в диагностике токсокароза являются иммунологические тесты. В настоящее время на кафедре тропических болезней РМАПО завершена работа по созданию диагностической иммуноферментной тест-системы «Тиаскар», которая прошла государственные испытания и выпускается АО «Вектор-Бест». Установлена корреляция между клиническими проявлениями, тяжестью процесса и титрами антител. На этом основании был сделан вывод о том, что в данной реакции титр специфических антител 1:800 и выше с большой степенью вероятности свидетельствует о заболевании, а титры 1:200, 1:400 — о носительстве токсокар при висцеральном токсокарозе и патологическом процессе при токсокарозе глаза.
За лицами с низкими титрами противотоксокарных антител при наличии показаний следует установить диспансерное наблюдение и при появлении клинических признаков болезни провести специфическую терапию. Учитывая то обстоятельство, что токсокароз может протекать в виде как субклинических, так и очень тяжелых клинических форм, представляется важным оценить удельную диагностическую значимость каждого отдельного признака токсокароза в баллах
Дифференциальный диагноз токсокароза следует проводить, прежде всего, с ранней стадией гельминтозов, свойственных человеку (аскаридоз, стронгилоидоз, шистосомозы, описторхоз и др.), а также многочисленными заболеваниями, сопровождающимися эозинофилией (синдром Леффлера, тропическая эозинофилия, хронический неспецифический полиартрит у детей, лимфогранулематоз, рак, медикаментозная сенсибилизация, пристеночный фибропластический миокардит и др.).
Таблица 1
Диагностическая ценность клинических признаков висцерального токсокароза в баллах
(по L.T. Glickman, 1978)
Признаки / Диагностическая ценность в баллах
1. Эозинофилия периферической крови 5 баллов
2. Лейкоцитоз 4
3. Увеличение СОЭ 4
4. Гипер—глобулинемия 3
5. Гипоальбуминемия 3
6. Анемия 2
7. Рецидивирующая лихорадка 3.5
8. Легочный синдром 3.5
9. Рентгенологические признаки поражения легких 2
10. Увеличение размеров печени 4
11. Неврологические расстройства 1.5
12. Кожные поражения 1
13. Лимфаденопатия 1
При сочетании симптомов и признаков, превышающих в сумме 12 баллов, предположение о токсокарозе можно считать достаточно клинически обоснованным, чтобы обследовать больного на токсокароз иммунологическим методом.
Существенное значение в постановке диагноза токсокароза имеет эпидемиологический анамнез. Указание на содержание в семье собаки или на тесный контакт с собаками, наличие привычки пикацизма свидетельствуют об относительно высоком риске заражения токсокарозом. Наличие аллергии на шерсть животных также часто встречается при токсокарной инвазии.
Лечение. Проблема специфической терапии токсокароза не может считаться решенной. Удовлетворительные результаты получают при назначении минтезола (тиабендазола), вермокса (метобендазола) и дитразина (диэтилкарбамазина).
Минтезол обычно назначают из расчета 25-50 мг на 1 кг массы тела в сутки в течение 5-10 дней подряд. Наблюдаемые побочные явления, связанные с влиянием минтезола, кратковременны и быстро проходят после отмены препарата. К ним относятся ухудшение аппетита, тошнота, головные боли, сонливость, боли в животе. Препарат быстро всасывается из желудочно-кишечного тракта и выводится почками. Не отмечено его отрицательного влияния на сердечно-сосудистую систему и органы дыхания.
Вермокс назначают независимо от возраста по 100 мг 2 раза в сутки в течение 2-4 нед. Взрослым иногда суточную дозу увеличивают до 300 мг. Побочные явления (боли в животе, тошнота, диарея) возникают крайне редко.
Дитразин цитрат назначают из расчета 2-6 мг на 1 кг массы тела в сутки в течение 2-4 недель. При лечении могут возникнуть побочные реакции: головная боль, головокружение, тошнота, иногда лихорадка.
Мы использовали для лечения больных в 1988-1990 гг. альбендазол фирмы «Смит Клайн Френч» (Великобритания), который назначали из расчета 10 мг/кг массы больного в течение 10-20 дней. Во время приема препарата редко возникали боли в животе, тошнота, диарея, которые исчезали после его отмены.
Изучение сравнительной эффективности для лечения висцерального и глазного токсокароза тиабендазола и альбендазола, проведенное в 1989 в Цюрихе (D. Sturchler, P. Schubarth) показало высокую эффективность обоих препаратов при применении их в дозе 10 мг/кг массы в течение 5 суток. При возможности авторы рекомендуют предпочтение отдавать альбендазолу. Поскольку эти препараты обладают тератогенным эффектом, их не следует применять для лечения беременных.
Побочные явления, возникающие при применении вышеуказанных препаратов, могут быть связаны не только с токсическим действием антигельминтных препаратов, но и с реакцией организма на гибель личинок токсокар. Поэтому в процессе лечения целесообразно назначать также антигистаминные средства.
Критериями эффективности лечения следует считать прогрессивное снижение уровня эозинофилии, регресс клинических проявлений болезни, снижение уровня специфических антител до уровня 1:800 и ниже. При медленном улучшении клинико-лабораторных показателей курсы специфической терапии проводят через 3-4 мес. Иногда требуется 4-5 курсов лечения.
Лечение глазного токсокароза впервые успешно было проведено в 1968 г. Девочку 13 лет с периферической гранулемой и помутнением стекловидного тела излечили субконъюнктивальными инъекциями депомедрола. Некоторые специалисты не отмечают эффекта от применения кортикостероидов. Ряд специалистов рекомендует применение противогельминтных препаратов по тем же схемам, как при висцеральном токсокарозе, назначение комбинированных курсов специфической терапии. Имеются сообщения об успешном использовании фото- и лазерокоагуляции для разрушения токсокарных гранулем. В некоторых случаях лечение глазного токсокароза осуществляется хирургическими методами. Описано (W. Kent, W. Brooks et al., 1989) успешное излечение 12 пациентов с диагнозом глазного токсокароза (повышенные титры противотоксокарных антител выявлены у 11) с помощью витрэктомии. У всех больных гранулемы располагались в заднем поле или по периферии сетчатки.
Прогноз при токсокарозе в большинстве случаев благоприятный. Однако, при интенсивной инвазии и проникновении личинок в жизненно важные органы заболевание может привести к летальному исходу.
Продолжение позже.
 И снова ОРВИ, ОРЗ, грипп, пневмония
И снова ОРВИ, ОРЗ, грипп, пневмония  А вот так внезапно. Зорицвет. Маклейя и чистотел. Атерома. Дискинезия. Кора осины
А вот так внезапно. Зорицвет. Маклейя и чистотел. Атерома. Дискинезия. Кора осины  Профилактика варикоза
Профилактика варикоза 











Паразиты. Токсокароз, часть 1{0}
Продолжение.
Паразиты. Энтеробиоз, трихоцефалез, капилляриоз.
Паразиты. Стронгилоидоз, гнатостомоз, аскаридоз.
Паразиты. Нематоды.
Helicobacter Pylori, часть 2
Helicobacter Pylori, часть 1
Рак и СПИД
Профилактика и подготовка к терапии
Заболевания вызванные паразитами
Симптомы наличия паразитов в организме
Паразиты – кто они?
Начало.
Токсокароз
Токсокароз является заболеванием, о котором, несмотря на широкое распространение и важную роль в патологии, особенно у детей, практические врачи знают весьма немного. Симптоматика его очень разнообразна, поэтому с ним могут встретиться врачи самых разных специальностей: педиатры, терапевты, окулисты, гематологи, гастроэнтерологи, невропатологи и другие.
Еще в 1911 г. F. Fulleborn высказал предположение о возможности паразитирования у человека несвойственных ему видов аскаридат с развитием аллергических реакций. В 1952 г. P. Beaver назвал феномен миграции личинок гельминтов животных у человека «larva migrans» (мигрирующие личинки) и утвердил этот термин как диагностическую единицу. «Larva migrans» – это большая группа зоонозных болезней, характеризующаяся следующими особенностями:
человек для их возбудителя – несвойственный хозяин;
возбудители в организме человека не достигают половозрелого состояния;
симтомокомплекс обусловлен миграцией личинок или взрослых гельминтов в коже или внутренних органах человека.
В зависимости от преобладающих симптомов выделяют кожную, висцеральную и глазную формы larva migrans. Позднее, в 1969 г., P. Beaver предложил в тех случаях, когда известен возбудитель, обозначать заболевание не расплывчатым термином «мигрирующая личинка», а конкретным названием, происходящим от названия возбудителя (дирофиляриоз, гнатостомоз, ангиостронгилез, капиляриоз, спарганоз и др.). Инвазию, вызываемую аскаридатами собак (Toxocara canis), он назвал токсокарозом.
Морфология и жизненный цикл возбудителя
Возбудитель токсокароза – нематода семейства Anisakidae (Skrjabin et Korokhin, 1945) рода Toxocara (Stiles, 1905). Известны три вида токсокар: Tocsocara canis (Werner, 1782) – гельминт, поражающий главным образом представителей семейства псовых, Toxocara mystax (Zeder, 1800) — гельминт семейства кошачих, который иногда в англоязычных странах называют Tocsocara cati и Toxocara vitulorum (гельминт, поражающий коров) роль которого пока не изучена
Роль Т. canis в патологии человека доказана, а роль Т. mystax еще обсуждается, поэтому в настоящее время термин «токсокароз» подразумевает только заболевание человека, вызываемое Toxocara canis.
Toxocara canis – нематода, самка которой имеет длину 6-8 см, самец – 4-10 см. Одним из важных дифференциальных морфологических признаков токсокар являются вздутия кутикулы на головном конце, образующие боковые крылья размером 2.3 на 0.3 мм.
Яйца токсокар почти круглой формы. Они крупнее оплодотворенных яиц аскарид – соответственно 65-75 и 50-70 мкм. Наружная оболочка яиц толстая, плотная, мелкобугристая, напоминающая поверхность наперстка, цвет ее – от светло-коричневого до темно-коричневого. Внутри незрелого яйца расположен шаровидный темный бластомер, заполняющий почти все яйцо. В зрелом яйце содержится живая личинка.
Т. canis обычно паразитирует у собак, волков, лисиц, песцов и других представителей семейства псовых. Взрослые паразиты локализуются в тонком кишечнике и желудке облигатных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4 мес., максимальная 6 мес. Самка Т. canis откладывает более 200 тыс. яиц в сутки. Поскольку зараженное животное носит в себе целую колонию токсокар, оно загрязняет окружающую среду миллионами яиц в сутки.
Яйца выделяются незрелыми (на стадии развития одного бластомера). Срок созревания яиц зависит от температуры окружающей среды и влажности. Зрелое яйцо содержит личинку, совершившую две линьки. В почве яйца длительное время сохраняют жизнеспособность. Широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
Для человека токсокароз – зоонозная инвазия. Она характеризуется тяжелым, длительным и рецидивирующим течением, полиморфизмом клинических проявлений, обусловленных миграцией личинок токсокар по различным органам и тканям. Заражение человека происходит при проглатывании зрелых яиц токсокар. В проксимальном отделе тонкого кишечника из яиц выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца. Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают пункта, где диаметр сосуда их не пропускает (диаметр личинки 0,02 мм), и здесь они покидают кровяное русло. Личинки токсокар оседают в печени, легких, сердце, почках, поджелудочной железе, головном мозге, глазах и других органах и тканях. Здесь они сохраняют жизнеспособность в течение длительного времени (месяцы, годы). Личинки, осевшие в тканях, пребывают в «дремлющем» состоянии, а затем под влиянием каких-то факторов активизируются и продолжают миграцию. С течением времени часть личинок инкапсулируется и постепенно разрушается внутри капсулы.
Патогенез и патология
Мигрируя в организме человека, личинки травмируют ткани, оставляя геморрагии, некрозы, воспалительные изменения. В секретах и экскретах личинок содержатся вещества, обладающие антигенной активностью (экзоантигены). Соматические антигены (эндоантигены) попадают в организм человека после разрушения личинки. Антигенное воздействие вызывает развитие аллергических реакций немедленного и замедленного типа. Судя по клинико-лабораторным показателям, поступление антигенов в организм человека происходит неравномерно и усиливается при возобновлении миграции после выхода из «дремлющего» состояния либо после гибели паразита.
В развитии аллергической реакции немедленного типа первый момент встречи организма человека с личинкой не вызывает видимых проявлений, основные клинические симптомы связаны со второй фазой, так называемой «реакцией поздней фазы» в виде отека, эритемы кожи и увеличения резистентности дыхательных путей к вдыхаемому воздуху. В «реакции поздней фазы» принимают участие тучные клетки, базофилы, а также нейтрофилы. В это время повышается уровень гистамина и хемотаксического фактора нейтрофилов и других клеток.
Основную роль в механизме противопаразитарного иммунитета играют эозинофилы. Эти клетки осуществляют защиту организма человека в содружестве с иммуноглобулином Е, уровень которого неизменно повышается при токсокарозе, а также с тканевыми базофилами, макрофагами. Как известно, пролиферация эозинофилов регулируется Т-лимфоцитами.
Механизм привлечения эозинофилов очень сложен и многократно дублируется. В нем принимают участие лимфокины, выделяемые сенсибилизированными лимфоцитами, низкомолекулярный хемотаксический фактор, продуцируемый нейтрофилами при взаимодействии их с иммунными комплексами, лейкотриены, продуцируемые лимфоцитами, нейтрофилами, тканевыми базофилами.
Тканевые базофилы у человека находятся в слизистых оболочках, коже, легких. На пути миграции личинки токсокар постоянно соприкасаются с этими и другими клетками.
Количество тканевых базофилов зависит от степени сенсибилизации организма антигенами. Тканевые базофилы выделяют активные амины (гепарин, гистамин), которые препятствуют свертыванию крови, расширяют сосуды, способствуют миграции клеток в очаг повреждения. В сочетании с лейкотриенами и другими медиаторами они вызывают основные клинические симптомы аллергии: гиперемию, зуд кожи, крапивницу, бронхоспазм, что и характерно для токсокароза.
Процесс освобождения активных аминов происходит при соединении IgE-антител с антигенными детерминантами клеток, активации комплемента, агрегации тромбоцитов или активации кининовой системы, что, по-видимому, приводит к тромбоцитопении при токсокарозе. Полинуклеары на фоне этого процесса повреждают мелкие кровеносные сосуды. При этом выделяются эндогенные пирогены, которые часто вызывают повышение температуры тела. Иммунные комплексы привлекают в очаг поражения эозинофилы, в результате чего образуются эозинофильные инфильтраты. Эозинофилы частично разрушают иммунные комплексы, смягчая этим тяжесть патологических реакций в тканях.
Реакция иммунных комплексов, наряду с выше указанными факторами, ответственна за формирование лихорадочной реакции, крапивницы, генерализованной лимфаденопатии.
Сенсибилизированные Т-лимфоциты, скопившиеся вокруг личинки, выделяют лимфотокины, привлекают и активируют макрофаги и другие клетки, которые включаются в процесс формирования гранулем.
Гранулемы при токсокарозе могут образовываться в любом органе и ткани за счет механизмов реакции замедленного типа. В центре гранулемы имеется зона некроза, по периферии — большое количество эозинофилов, а также гистоциты, нейтрофилы, лимфоидные, эпителиоидные клетки и макрофаги. Многочисленные гранулемы при токсокарозе находятся в печени, легких, а также в поджелудочной железе, миокарде, мезентериальных лимфатических узлах, головном мозге.
Таким образом, гистоморфологически токсокароз представляет собой диссеминированный эозинофильный гранулематоз как проявление аллергической реакции замедленного типа.
Заражение паратенических хозяев зрелыми яйцами токсокар приводит в течение нескольких дней к поражению печени с выраженной эозинофильной инфильтрацией интерстициальной ткани. В печени при этом образуется много гранулем с личинками и без них. Позднее по периферии клеточного слоя гранулемы с личинкой образуется фиброзная капсула. Так же быстро формируются гранулемы в легких, что приводит к гиперемии и отеку легочной ткани, активной лимфоидной реакции, а затем к возникновению пневмонии и альвеолита. В течение первых дней после заражения личинки попадают в головной мозг, почки, мышцы и другие органы и ткани.
В селезенке развиваются пролиферативные изменения в фолликулах. В корковом слое почек образуются лейкоцитарные скопления с наличием множества эозинофилов, паразитарные гранулемы. В миокарде возникают клеточные инфильтраты и экстравазаты. По истечении первой недели после заражения число личинок в этих органах значительно снижается. Личинки сохраняют жизнеспособность многие месяцы и годы, а их распределение в органах и тканях продолжает меняться. Число личинок в печени значительно больше при суперинфекциях и реинфекциях, чем при заражении низкими дозами или при обычном первичном заражении. Все вышеперечисленное в какой-то степени происходит в организме человека, который также является паратеническим хозяином токсокар.
Личинка в организме человека может выживать до 10 лет. Эта, как бы противоречащая выраженному иммунному ответу хозяина жизнеспособность личинки связана с выделением ею маскирующей субстанции, способной защитить личинку от агрессии эозинофилов и антител хозяина при помощи сложной реакции, в результате которой предотвращается их контакт с эпикутикулой личинки.
Формирование иммунного ответа – основной защитной реакцией организма – является главным механизмом патогенеза гельминтов вообще, и токсокароза в частности. Иммунологические реакции, переходя границы адекватного иммунного ответа, становятся иммунопатологическими и являются причиной формирования патологического процесса.
Следовательно, все патологические проявления при токсокарозе связаны в основном с аллергическими реакциями немедленного и замедленного типа. Однако, остается еще много неразрешенных вопросов в патогенезе токсокароза, например, механизм возникновения токсокароза глаз. Одна из гипотез высказана L.T. Glickman и P.W. Schantz, которые считают, что при низкой интенсивности инвазии личинками токсокар, суммарное антигенное воздействие на организм недостаточно, чтобы вызвать развитие аллергических реакций, гранулематозные процессы, эозинофилию, поэтому личинки свободно мигрируют по органам и тканям и попадают в органы зрения. При интенсивном заражении личинки попадают в «ловушку» иммунной и воспалительной реакций. Но на этом фоне иммунной защиты могут развиваться не только висцеральная форма, но и сочетанная патология в виде висцерального и глазного токсокароза одновременно.
Клиника
Спектр клинических проявлений зависит от интенсивности заражающей дозы, частоты реинфекций, распространения личинок в тех или иных органах и тканях, а также степени иммунного ответа хозяина. Токсокароз характеризуется длительным рецидивирующим течением (от нескольких месяцев до нескольких лет), что связано с периодическим возобновлением миграции личинок токсокар. Редкие летальные случаи при токсокарозе связаны с миграцией личинок в миокард и важные в функциональном отношении участки центральной нервной системы.
Соотношение частоты различных клинических форм токсокароза изучено пока недостаточно, однако по данным Центра по борьбе с болезнями в США на висцеральный токсокароз приходится 20%, глазной – 67%, бессимптомный – 13% от общего числа зарегистрированных в 1981 г. случаев. В Словакии (1993) на висцеральный токсокароз приходится 36%, глазной – 26% случаев.
В последние годы было установлено (Лысенко А.Я., Фельдман Э.В., Рыбак Е.А.), что токсокароз у детей приводит к снижению эффективности вакцинации и ревакцинации против кори, дифтерии и столбняка. У незараженных детей средние показатели титров антител часто превышают защитный уровень еще до ревакцинации, тогда как у зараженных личинками токсокар этот уровень и после ревакцинации остается ниже защитного. По сравнению с другими гельминтозами (энтеробиоз, аскаридоз) T. canis обладает наиболее активным поливалентным иммуноподавляющим действием.
Висцеральный токсокароз
Висцеральным токсокарозом болеют как дети, так и взрослые, хотя у детей это заболевание встречается чаще. Развитие висцерального токсокароза происходит вследствие заражения большим числом личинок и ассоциируется, например, у детей, с привычкой брать землю в рот. Основными симптомами токсокароза являются рецидивирующая лихорадка, легочный синдром, увеличение размеров печени, лимфаденопатия, эозинофилия, гипергаммаглобулинемия.
По нашим данным, у больных токсокарозом детей температура повышается обычно в полдень или вечером, сопровождаясь небольшим ознобом. Температурная реакция, как правило, наблюдается в период легочных проявлений (62% случаев). Синдром поражения легких встречается у 65% больных висцеральным токсокарозом и варьирует в широких пределах: от катаральных явлений до тяжелых астмоидных состояний. У больных наблюдаются рецидивирующие катары, бронхиты, бронхопневмонии. Беспокоит сухой кашель, частые приступы ночного кашля, в некоторых случаях – тяжелая одышка с астматическим дыханием и цианозом. При аускультации выслушиваются сухие, нередко влажные хрипы. При токсокарозе известны случаи развития тяжелых пневмоний, которые протекали с осложнениями и заканчивались летальными исходами. У нескольких больных, находящихся под нашим наблюдением и длительно страдавших бронхиальной астмой, удалось установить токсокарозную этиологию болезни, выявив высокий уровень специфических антител. Повторные курсы специфической терапии привели к купированию специфических проявлений болезни и постепенному полному выздоровлению. Подобное исследование, проведенное в Нидерландах, показало, что среди детей больных бронхиальной астмой или рецидивирующим бронхитом токсокароз выявляется с частотой 19.2% (в контрольной группе – 9.9%).
При рентгенологическом исследовании по нашим данным у 33.2% больных выявляются множественные или единичные эозинофильные инфильтраты, усиление легочного рисунка, картина бронхолёгочной инфильтрации.
Наряду с синдромом поражения легких очень часто (до 80 % по нашим наблюдениям) отмечается увеличение размеров печени. Печень при пальпации уплотнена, гладкая, часто напряженная. Примерно у 20 % больных увеличена селезенка, у 67 % – лимфатические узлы, вплоть до системной лимфаденопатии, особенно часто у детей. Лимфоузлы небольшого размера, безболезненные, не спаяны с окружающими тканями.
Кроме перечисленных проявлений у 46% наблюдаемых нами больных отмечался абдоминальный синдром (боли в животе, вздутие живота, тошнота, иногда рвота, диарея).
У 32 больных заболевание сопровождается разнообразного типа рецидивирующими высыпаниями на коже (эритематозные, уртикарные). Пальпаторно в местах высыпаний обнаруживаются небольшие уплотнения. Обследование на токсокароз детей с диагнозом «экзема», проведенное во время уже упомянутого исследования в Нидерландах, показало, что среди них 13.2 % имеют высокие титры специфических антител к токсокарам.
В отдельных случаях токсокароз протекает с развитием миокардита, по-видимому, аллергической природы. Описаны также эозинофильные панкреатиты, различные поражения почек, эозинофильные гранулемы в слизистой прямой кишки.
В последнее время некоторые исследователи наряду с висцеральным и глазным выделяют неврологическую форму токсокароза. При миграции личинок токсокар в головной мозг выявляются признаки поражения центральной нервной системы в виде конвульсий типа «petit mal», эпилептиформных припадков, парезов и параличей. Следует отметить, что частота высоких титров противотоксокарных антител у пациентов с эпилептическими припадками выше, чем в контрольной группе здоровых лиц, однако она одинакова у тех, у кого причина эпилептических припадков известна и неизвестна. Скорее всего, эпилепсия является не следствием, а лишь предрасполагающим к заражению токсокарозом фактором. Заражение токсокарозом вызывает также различные неврологические нарушения, проявляющиеся в изменении поведения: гиперактивность и аффекты в широком спектре поведенческих реакций – обучение, исследование внешней среды, решение комплекса проблем по выходу из сложной ситуации. Увязка таких явлений непосредственно с токсокарозом весьма проблематична, однако в одном из исследований показана связь затруднений при чтении, невозможности сосредоточиться и низкого уровня интеллекта с заболеванием дошкольников токсокарозом (1984 г.). Проведенное в Нью-Йорке обследование детей 1-15 лет показало, что инвазированные токсокарами дети имели существенные отклонения от здоровых детей во многих нейропсихологических тестах, моторной и познавательной функции.
Глазной токсокароз
Развитие глазного токсокароза связывают с заражением человека минимальным количеством личинок. Пациенты с глазным токсокарозом обычно старше, чем с висцеральным, иммунный ответ на заражение не так ярок, титры специфических противотоксокарных антител у них, как правило невысокие.
Первые случаи глазного токсокароза были выявлены в начале 50-х гг. нашего столетия, когда H. Wilder, проведя гистологическое исследование 46 глаз, энуклеированных у детей в связи с ретинобластомой (24 случая), болезнью Коатса, эндофтальмитом, в 24 случаях обнаружил личинки нематод или гиалиновые капсулы. Характерным изменением был эозинофильный абсцесс с некротическим центром. В 20 из этих 24 случаев заболевание клинически расценивалось как ретинобластома. В последующем токсокароз глаза начали диагностировать в разных странах с достаточным постоянством. Клинически у детей заболевание проявляется в виде косоглазия, снижения зрения, лейкокории. Личинки могут быть обнаружены при офтальмологическом исследовании, например, в области зрительного нерва или макулярной области.
Все случаи токсокароза глаза подразделяются на 2 основные группы: солитарные гранулемы и хронические эндофтальмиты с экссудацией. Практически всегда токсокарозом поражается только один глаз. При глазном токсокарозе обнаруживают, как правило, не более одной личинки.
Своеобразную форму поражения глаз при токсокарозе описали Hogan и соавторы в 1965 г. Личинка была обнаружена на периферии сетчатка у ребенка с хроническим парс-планитом. В стекловидном теле находился экссудат в виде «снежных шаров».
По данным некоторых авторов (Perkins, 1966) 10 % случаев хронического увеита связано с токсокарозом глаза.
В некоторых случаях (например, при интраретинальной миграции личинки) во время офтальмоскопии можно заметить движение личинки, а у пациента в поле зрения возникает мигрирующая скотома.
Поражение зрительного нерва личинкой токсокары может привести к односторонней слепоте. При этом диск и окружающая сетчатка инфильтруются лимфоцитами и эозинофилами, плазматическими клетками. Суммируя имеющиеся данные о поражении глаз при токсокарозе офтальмолог В.М. Чередниченко (1985 г.) выделяет следующие их формы:
гранулемы в заднем отделе глаза,
периферические гранулемы,
увеит,
парс-планит,
хронический эндофтальмит,
абсцесс в стекловидном теле,
неврит зрительного нерва,
кератит,
мигрирующие личинки в стекловидном теле.
В большинстве публикаций глазной токсокароз описан у детей.
Надежных методов диагностики глазного токсокароза не существует. Во многих случаях диагноз выясняется только при гистологическом исследовании. Brown (1970) сообщил, что из 245 энуклеированных им глаз в связи с диагнозом ретинобластомы, в 88 (35.9 %) обнаружена личинка токсокары. Дополнительными методами диагностики глазного токсокароза являются иммунологические реакции (которые не всегда в случаях глазного токсокароза бывают информативными), ультразвуковое и рентгенографическое исследование. В 1977 г. предложено в сомнительных случаях ретинобластомы проводить серологическое исследование на токсокароз пунктата передней камеры, а в 1979 г. — биоптата стекловидного тела.
Распространённость Токсокароза. Нами проведены расчеты оценочного числа лиц, больных висцеральным токсокарозом в РФ. Ожидаемое число больных среди детей в возрасте до 14 лет составляет 184 тыс. человек, в возрастной группе старше 14 лет – 366 тыс. Всего расчетное число больных токсокарозом может быть близким к цифре 550 тыс. человек, что составляет 380 на 100 тыс. населения. Для сравнения напомним, что аналогичный показатель при аскаридозе в 1993 г. составил 71.8.
Совершенно очевидно, что глазной токсокароз еще более недовыявляется, чем висцеральный. Это следует из сравнения с данными в США, где среди 700-1000 ежегодно регистрируемых Центром по борьбе с болезнями случаев токсокароза (по мнению специалистов Центра, эти сведения далеко не полные) на глазной токсокароз приходится 500-600 случаев, т.е. 67 %.
Лабораторные показатели. Одним из ведущих и наиболее постоянных проявлений висцеральной формы токсокароза является стойкая длительная эозинофилия вплоть до развития эозинофильно-лейкемоидных реакций крови. Обычно относительный уровень эозинофилов превышает 30%, а в отдельных случаях может достигать 90%. Высокий уровень эозинофилии отмечается также в некоторых случаях глазного токсокароза (до 44 %), но в целом она менее выражена и не столь постоянна. Общее количество лейкоцитов также повышается до 15-20х109/л, а в некоторых случаях – до 80х109/л. Эозинофилия может сохраняться в течение нескольких месяцев и даже лет.
По нашим данным, у больных висцеральной формой токсокароза (детей и взрослых) заболевание протекало с высокой эозинофилией периферической крови и у многих с повышением содержания лейкоцитов. По тяжести течения болезни можно выделить субклиническое, легкое и среднетяжелое, причем заболевание обычно протекает тяжелее у детей по сравнению со взрослыми. Средние показатели содержания лейкоцитов и эозинофилов у детей и взрослых различаются, имеется также тенденция к их увеличению по мере утяжеления течения болезни. Если содержание эозинофилов при субклиническом течении токсокароза у детей колебалось от 8 до 37%, при легком – от 12 до 74%, при среднетяжелом – от 20 до 80%, при тяжелом – от 60 до 79%, то у взрослых в этих же группах выявлены еще более высокие показатели. Так, при субклиническом течении токсокароза эозинофилия у взрослых составляла от 8 до 80%, при легком течении – от 13 до 84%, а при среднетяжелом – от 39 до 85%. Многие исследователи отмечают, что при прочих равных условиях у детей с токсокарозом уровень эозинофилии бывает выше, чем у взрослых.
В пунктате костного мозга выявляется эозинофильная гиперплазия, СОЭ обычно повышена, иногда значительно. При длительном течении болезни постепенно усиливается анемизация больных, уменьшается число эритроцитов, снижается уровень гемоглобина. Уровень общего белка сыворотки крови возрастает за счет глобулинов. В раннем периоде болезни преобладают иммуноглобулины класса М, позднее выявляются иммуноглобулины класса G. Особенно резко нарастает уровень иммуноглобулинов класса Е, который превышает норму у отдельных больных в 25-30 раз. При токсокарозе глаза эти явления выражены не столь ярко и могут отсутствовать.
Диагностика. Прижизненный паразитологический диагноз токсокароза практически невозможен, поскольку обнаружить мигрирующие личинки трудно, а идентифицировать их по гистологическим срезам весьма непросто. Тем не менее, окончательный паразитологический диагноз токсокароза ставят без сомнений только при обнаружении личинок в биоптатах тканей. Ограниченная возможность паразитологической диагностики приводит к тому, что ведущими в диагностике токсокароза являются иммунологические тесты. В настоящее время на кафедре тропических болезней РМАПО завершена работа по созданию диагностической иммуноферментной тест-системы «Тиаскар», которая прошла государственные испытания и выпускается АО «Вектор-Бест». Установлена корреляция между клиническими проявлениями, тяжестью процесса и титрами антител. На этом основании был сделан вывод о том, что в данной реакции титр специфических антител 1:800 и выше с большой степенью вероятности свидетельствует о заболевании, а титры 1:200, 1:400 — о носительстве токсокар при висцеральном токсокарозе и патологическом процессе при токсокарозе глаза.
За лицами с низкими титрами противотоксокарных антител при наличии показаний следует установить диспансерное наблюдение и при появлении клинических признаков болезни провести специфическую терапию. Учитывая то обстоятельство, что токсокароз может протекать в виде как субклинических, так и очень тяжелых клинических форм, представляется важным оценить удельную диагностическую значимость каждого отдельного признака токсокароза в баллах
Дифференциальный диагноз токсокароза следует проводить, прежде всего, с ранней стадией гельминтозов, свойственных человеку (аскаридоз, стронгилоидоз, шистосомозы, описторхоз и др.), а также многочисленными заболеваниями, сопровождающимися эозинофилией (синдром Леффлера, тропическая эозинофилия, хронический неспецифический полиартрит у детей, лимфогранулематоз, рак, медикаментозная сенсибилизация, пристеночный фибропластический миокардит и др.).
Таблица 1
Диагностическая ценность клинических признаков висцерального токсокароза в баллах
(по L.T. Glickman, 1978)
Признаки / Диагностическая ценность в баллах
1. Эозинофилия периферической крови 5 баллов
2. Лейкоцитоз 4
3. Увеличение СОЭ 4
4. Гипер—глобулинемия 3
5. Гипоальбуминемия 3
6. Анемия 2
7. Рецидивирующая лихорадка 3.5
8. Легочный синдром 3.5
9. Рентгенологические признаки поражения легких 2
10. Увеличение размеров печени 4
11. Неврологические расстройства 1.5
12. Кожные поражения 1
13. Лимфаденопатия 1
При сочетании симптомов и признаков, превышающих в сумме 12 баллов, предположение о токсокарозе можно считать достаточно клинически обоснованным, чтобы обследовать больного на токсокароз иммунологическим методом.
Существенное значение в постановке диагноза токсокароза имеет эпидемиологический анамнез. Указание на содержание в семье собаки или на тесный контакт с собаками, наличие привычки пикацизма свидетельствуют об относительно высоком риске заражения токсокарозом. Наличие аллергии на шерсть животных также часто встречается при токсокарной инвазии.
Лечение. Проблема специфической терапии токсокароза не может считаться решенной. Удовлетворительные результаты получают при назначении минтезола (тиабендазола), вермокса (метобендазола) и дитразина (диэтилкарбамазина).
Минтезол обычно назначают из расчета 25-50 мг на 1 кг массы тела в сутки в течение 5-10 дней подряд. Наблюдаемые побочные явления, связанные с влиянием минтезола, кратковременны и быстро проходят после отмены препарата. К ним относятся ухудшение аппетита, тошнота, головные боли, сонливость, боли в животе. Препарат быстро всасывается из желудочно-кишечного тракта и выводится почками. Не отмечено его отрицательного влияния на сердечно-сосудистую систему и органы дыхания.
Вермокс назначают независимо от возраста по 100 мг 2 раза в сутки в течение 2-4 нед. Взрослым иногда суточную дозу увеличивают до 300 мг. Побочные явления (боли в животе, тошнота, диарея) возникают крайне редко.
Дитразин цитрат назначают из расчета 2-6 мг на 1 кг массы тела в сутки в течение 2-4 недель. При лечении могут возникнуть побочные реакции: головная боль, головокружение, тошнота, иногда лихорадка.
Мы использовали для лечения больных в 1988-1990 гг. альбендазол фирмы «Смит Клайн Френч» (Великобритания), который назначали из расчета 10 мг/кг массы больного в течение 10-20 дней. Во время приема препарата редко возникали боли в животе, тошнота, диарея, которые исчезали после его отмены.
Изучение сравнительной эффективности для лечения висцерального и глазного токсокароза тиабендазола и альбендазола, проведенное в 1989 в Цюрихе (D. Sturchler, P. Schubarth) показало высокую эффективность обоих препаратов при применении их в дозе 10 мг/кг массы в течение 5 суток. При возможности авторы рекомендуют предпочтение отдавать альбендазолу. Поскольку эти препараты обладают тератогенным эффектом, их не следует применять для лечения беременных.
Побочные явления, возникающие при применении вышеуказанных препаратов, могут быть связаны не только с токсическим действием антигельминтных препаратов, но и с реакцией организма на гибель личинок токсокар. Поэтому в процессе лечения целесообразно назначать также антигистаминные средства.
Критериями эффективности лечения следует считать прогрессивное снижение уровня эозинофилии, регресс клинических проявлений болезни, снижение уровня специфических антител до уровня 1:800 и ниже. При медленном улучшении клинико-лабораторных показателей курсы специфической терапии проводят через 3-4 мес. Иногда требуется 4-5 курсов лечения.
Лечение глазного токсокароза впервые успешно было проведено в 1968 г. Девочку 13 лет с периферической гранулемой и помутнением стекловидного тела излечили субконъюнктивальными инъекциями депомедрола. Некоторые специалисты не отмечают эффекта от применения кортикостероидов. Ряд специалистов рекомендует применение противогельминтных препаратов по тем же схемам, как при висцеральном токсокарозе, назначение комбинированных курсов специфической терапии. Имеются сообщения об успешном использовании фото- и лазерокоагуляции для разрушения токсокарных гранулем. В некоторых случаях лечение глазного токсокароза осуществляется хирургическими методами. Описано (W. Kent, W. Brooks et al., 1989) успешное излечение 12 пациентов с диагнозом глазного токсокароза (повышенные титры противотоксокарных антител выявлены у 11) с помощью витрэктомии. У всех больных гранулемы располагались в заднем поле или по периферии сетчатки.
Прогноз при токсокарозе в большинстве случаев благоприятный. Однако, при интенсивной инвазии и проникновении личинок в жизненно важные органы заболевание может привести к летальному исходу.
Продолжение позже.
Категория: Гельминтоз, Куренков С.П. Метки: Токсокароз
Материал опубликован: 31.03.2016